Dysautonomie Vasculaire et Hypotension Orthostatique dans l'Amylose Cardiaque
Comprendre, diagnostiquer et prendre en charge
L’hypotension orthostatique (HO) liée à la dysautonomie vasculaire est une complication fréquente et potentiellement grave des amyloses cardiaques, en particulier dans les formes AL et ATTRv. Elle peut être le symptôme inaugural dans environ 10% des cas, conduisant à une errance diagnostique.
L’HO représente une urgence fonctionnelle avec un impact majeur sur :
- La qualité de vie (impossibilité de se verticaliser)
- Le pronostic (chutes, traumatismes, mort subite)
- L’autonomie des patients
Épidémiologie et Types d'Amylose

Physiopathologie
Mécanisme de l'hypotension orthostatique neurogène
En situation normale :
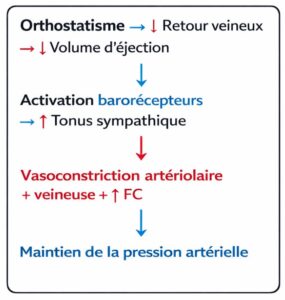
Dans l'amylose :

Caractéristique biologique : La norépinéphrine plasmatique est basse et ne s’élève pas à l’orthostatisme.
Le phénotype labile typique
L’alternance caractéristique :
- Hypertension de décubitus nocturne (nSH – neurogenic Supine Hypertension)
- Perte de la modulation autonome
- → Natriurèse nocturne
- → Aggravation de l’HO matinale
- Hypotension profonde en orthostatisme
- Incapacité à vasoconstricter
- Réponse chronotrope inadaptée
TA très dépendante : hydratation, repas, diarrhées, température, effort, douleur
Diagnostic
Définition de l'HO
Critères diagnostiques (après 3 minutes debout) :
PAS ↓ ≥ 20 mmHg OU
PAD ↓ ≥ 10 mmHg
⚠️ Attention : Symptômes très variables, parfois non ressentis malgré HO profonde.
Protocole de mesure standardisé
Étapes obligatoires :
1. Repos 3-5 min couché ou assis
2. Mesure TA/FC en décubitus
3. Mesure TA/FC debout à 1 minute
4. Mesure TA/FC debout à 3 minutes
5. Noter systématiquement les symptômes : vertiges, flou visuel, voile noir, faiblesse, nausées, douleur
épaules
Si station debout impossible : mesure TA/FC assise (moins sensible).
Confirmer l’origine neurogène : Ratio ΔFC/ΔPAS
Formule
Ratio = (FC debout – FC couché) / (PAS couché – PAS debout)
Exemple clinique :
Couché : PA 139/61 mmHg, FC 71 bpm
Debout 3 min : PA 89/42 mmHg, FC 74 bpm
ΔFC = 3 bpm ; ΔPAS = 50 mmHg
Ratio = 0,06 bpm/mmHg
Interprétation
| Ratio | Signification | Prise en charge |
| < 0,5 | HO neurogène (dysautonomie) | Traitement presseur |
| ≥ 0,5 | HO par hypovolémie ou bas débit | Réhydratation / Ajustement traitement cardiaque |
Limites : Stimulo-dépendant, fibrillation atriale, bétabloquants
Définir la sévérité (obligatoire)
HO SÉVÈRE
Malaises sévères et/ou syncopes au lever
Patient capable de tenir debout un minimum avec aide et traitement
⚠️ Risque élevé de chute, surtout la nuit (nycturie + syncope post-mictionnelle)
HO TRÈS SÉVÈRE
Syncope dès mise debout
Parfois syncope même assis
Confinement au lit temporaire jusqu’à stabilisation
Nécessite hospitalisation
Hypertension neurogène de décubitus (nSH)
Définition (consensus AAS/EFAS) :
- PAS ≥ 140 et/ou PAD ≥ 90 après ≥5 minutes couché
- Gradation : mild / moderate / severe
Conséquences
- Natriurèse nocturne → aggravation HO matinale
- Nycturie → risque de chute nocturne
⚠️ Ne JAMAIS traiter comme une HTA essentielle
Gestion
- Horaire midodrine adapté (arrêt 3-4h avant coucher)
- Inclinaison tête de lit 10-15°
Prise en Charge Thérapeutique
Mesures non pharmacologiques (FONDAMENTALES)
Bas de contention
Classe II (force 2) mi-cuisse ou collant
Mise en place A V ANT le premier lever
24h/24 dans les formes sévères
Alternative si intolérance : ceinture abdominale
Lever progressif
Protocole en 3 étapes :
1. Allongé → pause 30 sec
2. Assis bord du lit → pause 1 min
3. Debout avec appui → surveillance 5-10 min
⚠️ Attendre ≥ 1h après prise de midodrine
Inclinaison tête de lit 10-15°
Bénéfices majeurs :
↓ HTA de décubitus nocturne
↓ Natriurèse et pertes hydrosodées
↓ Nycturie → ↓ risque chute nocturne
↓ Hypovolémie matinale
Amélioration HO matinale
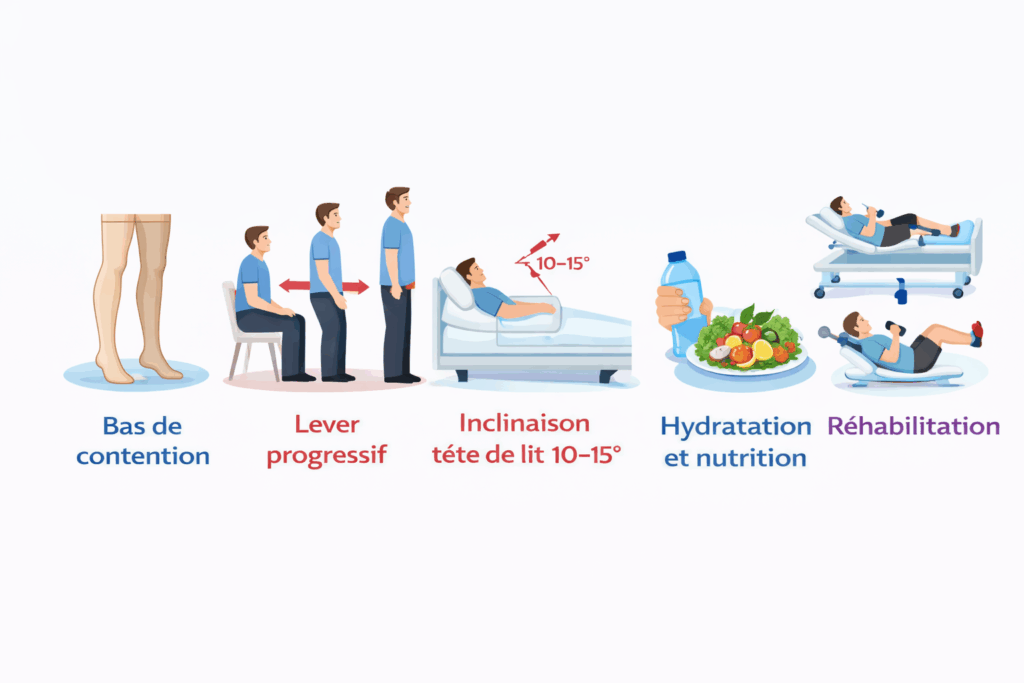
Hydratation et nutrition
Hydratation renforcée (adapter selon cardiopathie)
500 mL eau rapidement = effet pressif rapide (« rescue »)
Petits repas fréquents, moins glucidiques
Éviter alcool (vasodilatateur)
Sel selon avis
Réhabilitation
Pédalier de lit (limiter déconditionnement)
Exercices assis/couché
Éviter station debout prolongée
Traitement pharmacologique
MIDODRINE (GUTRON®) - Traitement de première ligne
Pharmacologie :
Demi-vie : ~3 heures
Délai d’action : 45-60 minutes
Durée d’action : 3-4 heures
Posologie :
Initiation : 2,5 mg × 4/jour
Titration : tous les 24-48h
Maximum : 10 mg × 4/jour (40 mg/jour)
Horaires types : 7h / 10h / 13h / 16h
Dernière prise ≥ 3-4h avant coucher (limite nSH)
⚡ Concept EFFET ON/OFF :
Prise → OFF (0-45 min) → Transition (45-60 min) → ON (1-4h) → OFF (>4h)
Conséquence pratique : Lever uniquement en phase ON (≥1h post-prise)
Précautions :
Surveillance TA couchée
Risque bradycardie réflexe
CI : HTA sévère non contrôlée, rétention urinaire
⚠️ Ne jamais interrompre même si patient à jeun pour examen
FLUDROCORTISONE (FLUCORTAC®) - Traitement adjuvant
Posologie :
Initiation : 50 µg/jour
Prise → OFF (0-45 min) → Transition (45-60 min) → ON (1-4h) → OFF (>4h)Dose usuelle : 100-200 µg/jour
Prise vespérale
Surveillance :
Kaliémie (hypokaliémie)
Poids, œdèmes (rétention hydrosodée)
TA couchée (aggravation nSH)
Précautions :
Éviter si IC droite sévère
Prudence si œdèmes/ascite
DROXIDOPA (DOPS OD®) - ATU - Si échec/intolérance
Indications :
Échec midodrine ± fludrocortisone
Intolérance midodrine
Association midodrine (formes très sévères – milieu spécialisé)
Posologie :
Initiation : 100 mg × 3/jour
Titration progressive
Maximum : 600 mg × 3/jour (1800 mg/jour)
Surveillance : HTA couchée, céphalées
📋 Formulaire ATU disponible sur www.reseau-amylose.org
Adaptation des traitements cardiovasculaires
À supprimer/adapter :
❌ Hypotenseurs
❌ Vasodilatateurs
⚠️ Diurétiques si possible (selon IC)
⚠️ Bétabloquants
Pacemaker :
Accélération FC de repos selon gravité
Effet isolé probablement faible
En complément des autres mesures
Protocole Hospitalier - Sécurité

Brancardage et examens (POINT CRITIQUE)
L’IDE doit prévenir :
Le brancardier
L’équipe d’examen (scanner, IRM, écho, endoscopie)
Message : »Patient HO sévère – Risque syncope – Ne pas lever sans bas + délai 1h post-GUTRON® – Transfert
assisté »
⚠️ Risque maximal : retour de salle (fatigue + hypovolémie)
Affichage en chambre
Outil de sécurité : Affiche visible alertant tout soignant entrant
HO sévère vs HO très sévère
Consignes de lever
Horaires GUTRON®
Éducation Thérapeutique
Objectif : Patient et aidants ACTEURS
Le patient doit pouvoir dire aux soignants :
💬 « Je ne peux pas être levé sans mes bas et sans délai après la midodrine »
💬 « Je peux faire une syncope si on me met debout trop vite »
💬 « Je dois être accompagné la nuit »
💬 « Ne modifiez pas mon traitement sans l’accord de mon équipe amylose »
Outils pédagogiques disponibles
Fiche patient/aidant
Fiche protocole soignants
Carte d’urgence dysautonomie
Affiche chambre
Triptyque explicatif
Vidéos éducatives
Tous les documents téléchargeables sur www.reseau-amylose.org
Complications et Pronostic
Impact clinique
À court terme :
Chutes et traumatismes (⚠️ risque majoré si anticoagulants)
Mort subite (désamorçage de la pompe)
Décès
À long terme :
Perte d’autonomie majeure
Altération qualité de vie (impossibilité verticalisation)
Alitement, déconditionnement, dénutrition
Hospitalisations prolongées et répétées
Impact pronostique
Données récentes :
L’HO impacte significativement la survie dans l’amylose AL (Sakhi et al. 2025)
Chez patients AL avec syndrome néphrotique + atteinte cardiaque :
16% présentent une dysautonomie
Impact pronostique majeur
Erreurs Fréquentes à Éviter
| ERREUR | CONSÉQUENCES |
| Mesurer uniquement TA couchée | Sous-diagnostic et sous-traitement |
| Lever < 1h après GUTRON® | Chute (effet OFF) |
| Bas non mis/mal adaptés | Chute |
| Traiter HTA couchée « classiquement » | Aggravation majeure HO |
| Oublier diarrhée/vomissements | Déshydratation → chute |
| Lever nocturne non assisté | Syncope post-mictionnelle |
| Arrêter GUTRON® si à jeun | Effet OFF → chute |
Cas Particuliers
Anesthésie et dysautonomie sévère
Risques majeurs :
Hypotension per-opératoire sévère
Allongement QT et ischémie
Réponse diminuée à hypoxémie/hypercapnie
Atropine souvent inefficace
Précautions
Information anesthésiste ++
Maintien midodrine jusqu’au bloc
Monitoring invasif
Vasopresseurs disponibles
Transplantation cardiaque
La dysautonomie sévère peut constituer une contre-indication relative à la greffe cardiaque.
Quand Contacter le Centre de Référence ?
Situations nécessitant avis spécialisé
| SITUATION | DÉLAI |
| HO très sévère (syncope dès lever) | 48h |
| Syncopes quotidiennes | 48h |
| Chutes répétées malgré traitement | 1 semaine |
| Aggravation brutale | Urgent |
| Impossibilité tenir debout/assis | 24h |
| Diarrhées/vomissements persistants | 2-3 jours |
Contact :
Centre de Référence Amylose Cardiaque – CHU Henri Mondor
📞 01.49.81.22.53
Algorithme Décisionnel
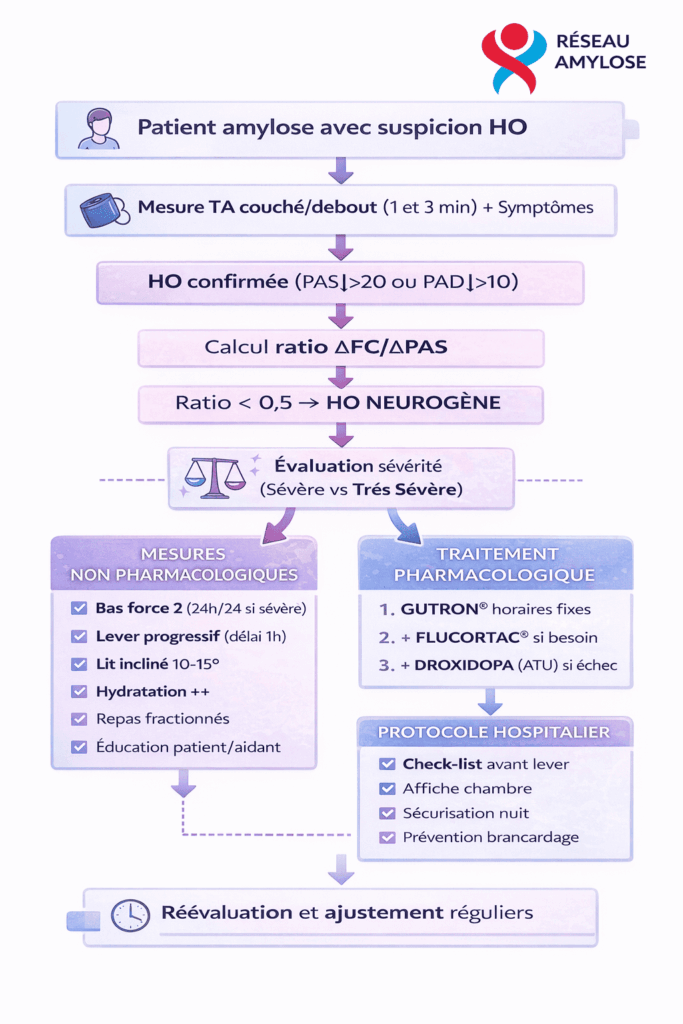
Ressources Téléchargeables
Pour les professionnels de santé
📄 Fiche protocole complet (format PDF)
📄 Triptyque « Prise en charge de l’HO dans l’amylose »
📄 Affiche chambre (HO sévère / HO très sévère)
📋 Formulaire ATU Droxidopa
🎥 Vidéo de formation « Les 6 gestes qui évitent une chute »
📊 Présentation PowerPoint (support formation)
Pour les patients et aidants
📄 Fiche patient/aidant « Vivre avec une dysautonomie »
💳 Carte d’urgence dysautonomie (format CB)
📖 Livret de suivi (TA, symptômes, horaires)
Bibliographie Sélective
Publications récentes - Dysautonomie dans l'amylose - 2025-2026
Barocelli F et al. The Vagal link: Autonomic Nervous System Dysfunction in Cardiac Amyloidosis. J
Clin Med. 2025;14(24):8963.
Iacovelli JJ et al. Attenuated Peripheral Vascular Responsiveness in wtATTR. Am J Physiol Heart Circ
Physiol. 2026 Jan 30.
Weinsaft A et al. Impact of autonomic dysfunction on cardiovascular outcomes in ATTR: insights from
COMPASS-31. Amyloid. 2025;32(4):314-323.
Sakhi H et al. Impact of autonomic dysfunction in light chain amyloidosis with nephrotic syndrome and
cardiac involvement. Amyloid. 2025;32(4):371-374.
Poledniczek M et al. Prevalence of Autonomic Dysfunction in Cardiac Amyloidosis. J Clin Med. 2025.
Consensus et guidelines
Fanciulli A et al. Consensus statement on neurogenic supine hypertension (AAS/EFAS). Clin Auton Res.
2018;28(4):355-362.
Palma JA et al. Orthostatic hypotension in hereditary transthyretin amyloidosis: epidemiology, diagnosis
and management. Clin Auton Res. 2019. PMID: 31452021.
González-Duarte A et al. Blood pressure and orthostatic hypotension in THAOS. Auton Neurosci. 2019.
PMID: 31726319.
Traitements
Valladares C et al. Droxidopa in Critical Care: A Systematic Review. Crit Care Res Pract.
2025;2025:4830160.
McDonell KE et al. Initiation of droxidopa for refractory neurogenic OH. J Clin Hypertens.
2019;21(9):1308-1314.
Ruiz Lopez JN et al. Droxidopa for Refractory OH in AL Amyloidosis. Blood. 2021;138(Suppl 1):4737.
Points Clés à Retenir
1. L’HO = urgence fonctionnelle avec impact majeur sur pronostic et qualité de vie
2. Ratio ΔFC/ΔPAS < 0,5 confirme l’origine neurogène
3. Définir la sévérité (sévère vs très sévère) guide la prise en charge
4. Mesures non pharmacologiques = fondamentales (bas, lever, lit incliné)
5. GUTRON® : effet ON/OFF → lever uniquement ≥1h après prise
6. HTA couchée ≠ HTA essentielle → ne jamais traiter classiquement
7. La nuit = période à haut risque (nycturie + syncope post-mictionnelle)
8. Brancardage/examens = point critique → prévenir systématiquement
9. Patient acteur → éducation fondamentale
10. Protocole hospitalier strict = prévention des chutes
